Osebne zbirke


Elektrofilne substitucije so reakcije značilne za benzenov obroč:
Delokalizirane vezi, značilne za aromatske spojine, so vir elektronske gostote in zato mesta bogata z elektroni. Taka mesta so idealna za napad elektrofilov.
Elektrofili so lahko:
pozitivno nabiti delci 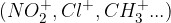 ,
,
neionski elektrofili 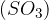 .
.
Da teke reakcije potečejo, je velikokrat potrebno segrevanje ali pa dodati katalizator. Pogoje reakcij si bomo natančneje pogledali na posameznih reakcijah.
Na benzenovem obroču so vsi ogljiki med seboj enakovredni in zato je (s stališča opisovanja reakcije) vseeno, na katerem se zgodi prva zamenjava z vodikom. Pri vseh nadaljnjih zamenjavah pa moramo biti pazljivejši, saj so z mestom, kjer se veže naslednja molekula, določene tudi lastnosti benzenovega obroča.
Za začetek si najprej poglejmo osnovne reakcije na benzenovem obroču. Poznamo sledeče reakcije:
nitriranje (nastane nitro skupina 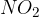 ),
),
sulfoniranje (nastane sulfonska skupina 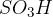 ),
),
halogeniranje (vodik se zamenja z halogenim elementom),
alkiliranje (vodik se zamenja z alkilno verigo),
aciliranje (vodik se zamenja z acilno skupino in nastanejo ketoni).
Poglejmo si podrobneje vsako reakcijo posebej.
Pri nitriranju benzenovega obroča nastane nitrobenzen. Reakcija poteče, če sta v reakciji prisotna:
reagent v obliki dušikove (V) kisline 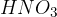 ,
,
katalizator v obliki žveplove (VI) kisline 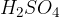
Pri reakciji nastane delec s pozitivnim nabojem 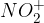 in ta napade benzenov obroč ter se nanj tudi veže.
in ta napade benzenov obroč ter se nanj tudi veže.
Mehanizem odcepa protona v benzenov obroč (glej gornji primer) se dogodi pri vseh elektrofilnih substitucijah in ga v nadaljevanju gradiva ne bomo posebej omenjali.
Pri sulfoniranju nastane benzensulfonska kislina. Reakcija poteče pod pogojem, če je prisotna:
žveplova (VI) kislina 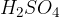 ,
,
nasičena s  (oleum).
(oleum).
Kislina deluje kot vir elektrofila in kot katalizator.
Pri reakciji delec s primanjkljajem elektronov  napade benzenov obroč ter se nanj veže. Pri tem vodik ni izrinjen iz molekule temveč samo spremeni pozicijo.
napade benzenov obroč ter se nanj veže. Pri tem vodik ni izrinjen iz molekule temveč samo spremeni pozicijo.
Pri halogeniranju nastane halogenobenzen. Da reakcija poteče, potrebujemo prisotnost:
reagenta v obliki halogenega elementa 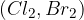 ,
,
katalizatorja v obliki aluminijevega trihalogenida (npr. 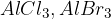 ) oziroma elektron deficitarno molekulo, ki spodbuja heterolitsko cepitev vezi.
) oziroma elektron deficitarno molekulo, ki spodbuja heterolitsko cepitev vezi.
Pri taki reakciji nastane delec s pozitivnim nabojem 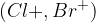 , ki napade benzenov obroč ter se nanj veže. Jod je posebnost: reakcija jodiranje ne poteče, saj je jod nereaktiven.
, ki napade benzenov obroč ter se nanj veže. Jod je posebnost: reakcija jodiranje ne poteče, saj je jod nereaktiven.
Pri alkiliranju nastanejo alkilbenzeni. Reakcija alkiliranja spada pod t.i. Friedel-Craftsove reakcije. Da reakcija poteče, potrebujemo:
reagent v obliki halogenoalkana (npr. klorometan 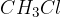 ),
),
katalizator, ki je 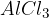 .
.
Pri reakciji nastane delec s pozitivnim nabojem 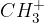 . Delec napade benzenov obroč ter se nanj veže. V tem primeru na nastane toluen.
. Delec napade benzenov obroč ter se nanj veže. V tem primeru na nastane toluen.
Aciliranje benzenovega obroča je podobno alkiliranju. Tudi v tem primeru reakcija spada pod t.i. Friedel-Craftsove reakcije. Da reakcija poteče, potrebujemo:
reagent v obliki alklaoil klorida (npr. acetil klorid 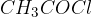 ),
),
katalizator v obliki 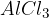 .
.
Pri reakciji nastane delec s pozitivnim nabojem 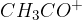 , ki napade benzenov obroč ter se nanj veže. V tem primeru nastane keton feniletanon.
, ki napade benzenov obroč ter se nanj veže. V tem primeru nastane keton feniletanon.
Skupine vezane na benzenov obroč spremenijo njegovo reaktivnost. Ogljiki si niso več enakovredni in posamezne skupine vplivajo, na katero pozicijo se bodo vezale vse nadaljne skupine. Substituente delimo v dve skupini:
Aktivirajoče skupine
Akitivirajoče skupine so skupine, ki stabilizirajo obroč in usmerjajo skupine, ki se naknadno vežejo na benzenov obroč, na orto in para pozicije (glej sliko 14).
Deaktivirajoče skupine
Deaktivirajoče skupine pa so tiste, ki destabilizirajo aromatski obroč. Slednje raje usmerjajo skupine, ki se naknadno vežejo na benzenov obroč, na meta pozicijo (glej sliko 21).
Aktivirajoče skupine se običajno vežejo na benzenov obroč preko najbolj elektronegativnega atoma in imajo možnost, da delijo z obročem svoje nevezane elektronske pare. Mednje sodijo:
aminske skupine 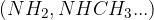
halogeni elementi 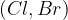
hidroksilna skupina 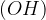
alkoksi skupina 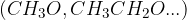
alkilne skupine 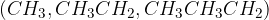
Če je ena izmed teh skupin vezana na benzenov obroč, bo naslednje skupine usmerjala na orto in para pozicijo na benzenovem obroču:
Pri takih reakcijah nastaneta dva produkta: v enem produkut je skupina vezana na orto, v drugem pa na para pozicijo.
V primeru alkilbenzenovih derivatov moramo biti precej pozorni pri halogeniranju spojine. Pazljivi moramo biti predvsem na reakcijske pogoje, saj lahko ob ustreznih pogojih poteče tudi radikalska substitucija na alkilni verigi.
Deaktivirajoče skupine se običajno vežejo na benzenov obroč preko najmanj elektronegativnega atoma. Posledica je, da bolj elektronegativni atomi v obroču privlačijo elektrone vezane skupine, s tem pa destabilizirajo reakcijski intermediat. Primeri skupin, ki se vežejo na najmanj elektronegativni atom, so:
ciano skupina 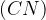
nitro skupina 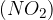
sulfonska skupina 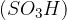
karboksilna skupina 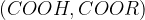
aldehidna in ketonska karbonilna skupina 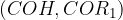
Če je ena izmed teh skupin vezana na benzenov obroč, bo novodošle skupine usmerjala na meta pozicijo benzenovega obroča: