Osebne zbirke


Atomi so sestavljeni iz (glej sliko 1):
jedra. Jedro pa je sestavljeno iz:
protonov - to so so delci, ki imajo pozitiven električni naboj;
nevtronov - to so delci, ki nimajo električnega naboja in so zato električno nevtralni.
elektronske ovojnice. Elektronska ovojnica je prostor, v kateri se nahajajo elektroni, ki so zelo majhni, lahki in negativno nabiti delci. Elektroni so tudi odgovorni za povezovanje atomov v molekule in snov.
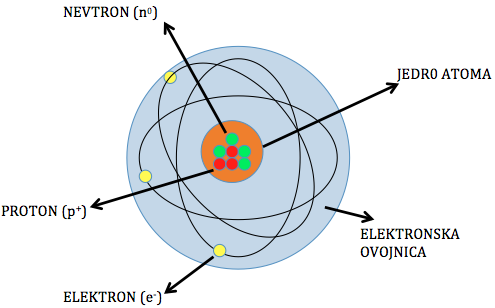
Slika 1: skica zgradbe atoma. Elektronski oblak ni nujno kroglast ampak se lahko elektroni gibljejo po različnih prostorskih razporeditvah, ki jih imenujemo elektronske orbitale.
Elektrone veže na jedro električna privlačna sila med njimi in protoni. Posamični atomi se pri tvorbi snovi vežejo v molekule, kristale in druge konfiguracije in pri tem procesu igrajo elektroni, natančneje električna sila med elektroni ključno vlogo, ter tako določajo lastnosti vseh snovi, ki jih lahko vidimo in občutimo.
Atomi so sestavljeni iz pozitivno nabitega jedra v katerem so protoni in nevtroni, ter negativno nabitih elektronov, ki sestavljajo zunanji plašč. Razporeditev in medsebojni vplivi elektronov določajo kemijske lastnosti atomov, molekul in kristalov.
Atoma je z nekoliko bolj kemijskega vidika obravnavan tudi v gradivu Delci v atomu.
Atomi se med sabo razlikujejo po številu elektronov, protonov in nevtronov, ki jih sestavljajo. Ta števila označimo kot:
Z - število protonov (imenujemo ga tudi vrstno število);
N - število nevtronov;
A - število protonov in nevtronov (imenujemo ga tudi masno število).
Velja torej:
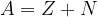
Atom je navzven električno nevtralen, zato je število elektronov enako številu protonov.
V periodni sistem atome razvrstimo po številu protonov v jedru:
na 1. mestu se nahaja element z enim protonom - vodik;
na 2. mestu v periodnem sistemu se nahaja element z dvema protonoma - helij;
....
na 8. mestu se nahaja element z osmimi protoni - kisik;
....
na 79. mestu se nahaja element z 79 protoni - zlato;
itd...
Prav zato, ker je število protonov tisto, ki določa vrstni red elementov v periodnem sistemu elementov, številu protonov rečemo tudi vrstno število. Atomom, ki imajo enako število protonov, rečemo, da pripadajo istemu elementu.
Ker so mase atomov zelo majhne, je uporabna enota za računanje t.i. atomska enota mase, ki jo označujemo z u in je enaka 1/12 mase ogljikovega izotopa 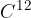 . Njena vrednost je:
. Njena vrednost je:
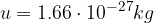
Masi protona in nevtrona sta si zelo podobni in sta zelo blizu atomski enoti mase u, medtem ko je masa elektrona precej manjša:
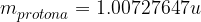
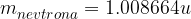
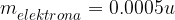
Ob primerjavi mas lahko opazimo, da je skoraj vsa masa atoma zbrana v jedru (mase elektronov so zanemarljive). Pri izračunih za maso atoma bomo tako pogosto privzeli, da je ta enaka vsoti mas protonov in nevtronov v jedru (elektronov ne bomo upoštevali).
Velikost atoma pa določa velikost elektronskih orbital, torej prostora po katerem se gibljejo elektroni. Ta prostor ni natančno določen, vendar lahko rečemo, da je povprečen polmer atoma 100 pikometrov, torej:
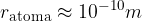
Samo jedro atoma pa je še 100.000 krat manjše: polmeri jeder so med 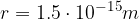 in
in 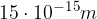 . Opazimo, da - čeprav je vsa masa atoma zbrana v jedru - skoraj ves volumen atoma predstavlja elektronska ovojnica.
. Opazimo, da - čeprav je vsa masa atoma zbrana v jedru - skoraj ves volumen atoma predstavlja elektronska ovojnica.