Osebne zbirke


Raztapljanje je proces, pri katerem se:
molekule ali ioni snovi, ki jo imenujemo topljenec,
enakomerno porazdelijo v drugi snovi, ki jo imenujemo topilo.
Raztopina je mešanica dveh ali več snovi in nastane pri raztapljanju. V raztopini topilo predstavlja večji del raztopine, topljenec pa manjši del.
Raztopina je zmes topila in topljenca.
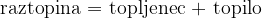
Topilo je snov, ki raztopi topljenec. Topilo je običajno v tekočem agregatnem stanju. Vendar pa obstajajo tudi raztopine, kjer je topilo v trdnem ali plinastem agregatnem stanju. Tukaj bomo obravnavali le raztopine, kjer je topilo v tekočem agregatnem stanju.
Topljenec je snov, ki se raztaplja v topilu. Lahko se nahaja v vseh treh agregatnih stanjih:
plinastem,
tekočem ali
trdnem.
Vendar pa v topilu ne moremo raztopiti poljubno velike količine topljenca. Raztaplja se le do določene mere. Največja količina topljenca v določenem topilu se imenuje topnost.
S topnostjo opišemo največjo količino topljenca, ki se lahko raztopi v nekem topilu pri dani temperaturi.
Topnost navajamo kot maso topljenca v 100 g topila (g snovi / 100 g topila) pri določeni temperaturi:
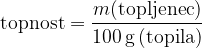
Kadar pripravljamo raztopino, želimo v topilu raztopiti določeno količino topljenca. Če dodamo veliko topljenca, se lahko zgodi, da se bo raztopil samo del topljenca, ostali topljenec pa bo ostal nespremenjen na dnu posode.
Glede na to, koliko topljenca je raztopljenega v raztopini, ločimo:
nasičene raztopine in
nenasičene raztopine.
Raztopina je nasičena, kadar vsebuje največjo možno količino raztopljenega topljenca pri določeni temperaturi.
Raztopina je nenasičena, kadar vsebuje manjšo količino raztopljenega topljenca, kot bi ga pri določeni temperaturi lahko vsebovala.
Največjo možno količino raztopljenega topljenca nam podaja topnost.
Na topnost vplivajo različni dejavniki:
topilo: snov ima lahko višjo topnost v nepolarnem topilu in nižjo topnost v polarnem topilu ali obratno;
topljenec: v določenem topilu se nekatere snovi zelo dobro topijo, drugih snovi pa v istem topilu ne moremo raztopiti;
temperatura: pri večini trdnih snovi se topnost poveča s povišanjem temperature, topnost plinov pa se s povišanjem temperature zmanjša.
Graf topnosti prikazuje, kako se topnost snovi spreminja s temperaturo. Na vodoravni osi je prikazana temperatura, na navpični osi pa količina snovi, ki se raztopi v določenem volumnu topila (običajno vode) pri določeni temperaturi.
Grafe topnosti uporabljamo, da lažje vidimo kako se topnost spreminja pri določenih temperaturah.