Osebne zbirke


Navajeni smo, da so kemijski elementi okoli nas stabilni. To pomeni, da če jih izoliramo od ostalega sveta, se s časom ne spreminjajo.
A to ne velja za vse elemente, saj so nekateri elementi nestabilni. To pomeni, da bi se elementi spremenili tudi, če bi jih popolnoma izolirali od okolice. Njihova nestabilnost ni posledica vplivov okolice, temveč je to lastnost elementov.
Če se izrazimo natančneje, so nestabilna jedra teh elementov. S tem imamo v mislih to, da jedra nestabilnih elementov s časom preidejo v stabilno stanje, pri tem pa oddajo delce ali pa sevanje. Proces, pri katerem jedra sama od sebe oddajajo različne delce ali sevanje, imenujemo radioaktivnost. Radioaktivnost je način, kako se nestabilna jedra z višjo energijo pretvarjajo v stabilna jedra z nižjo energijo.
Poznamo naslednje radioaktivne razpade jeder:
Alfa in beta razpad
Pri obeh razpadih se jedru zmanjša število protonov, začetni element pa se pretvori v nov element. Jedro pri razpadu odda delce ali pa sevanje.
Gama razpad
Pri gama razpadu se število protonov ne spremeni. Jedru se zmanjša:
notranje energijsko stanje ali
število nevtronov.
Jedro pri razpadu odda delce ali pa sevanje, element pa lahko - v primeru spremembe števila nevtronov - preide iz enega izotopa v drugega.
Proces razpada posameznih jeder je popolnoma naključen. Zato časa, kdaj bo določeno jedro razpadlo ni mogoče napovedati. Kar pa lahko napovemo, je, kako hitro bo razpadala množica (enakih) jeder. Namreč, vsaka radioaktivna snov ima svojo lastno hitrost razpadanja. Kot mero te hitrosti najpogosteje uporabljamo razpolovni čas.
Razpolovni čas, je čas, ki je potreben, da razpade polovica vseh začetnih jeder. Označimo ga s 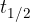 ali
ali 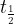 .
.
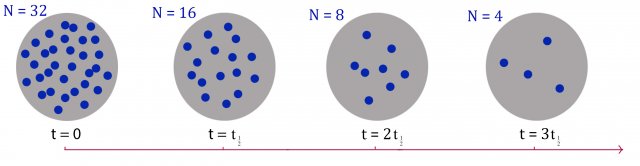
Slika 1: Razpadanje radioaktivnih jeder v odvisnosti od časa. Po preteku razpolovnega časa 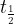 se število jeder vsakič zmanjša za polovico.
se število jeder vsakič zmanjša za polovico.
Razpolovni čas je tisti ključni podatek, s pomočjo katerega lahko izračunamo zmanjševanje števila jeder (N) s časom. Pri računanju uporabimo naslednjo enačbo:
Hitrost razpada radioaktivnih jeder izračunamo z:
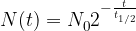
kjer je:
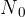 število vseh jeder ob začetku merjenja razpada;
število vseh jeder ob začetku merjenja razpada;
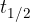 pa čas, v katerem razpade ena polovica začetnih jeder.
pa čas, v katerem razpade ena polovica začetnih jeder.
Včasih pri računanju razpada jeder uporabimo preoblikovano enačbo, v kateri namesto razpolovnega časa nastopa razpadna konstanta 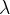 . Enačba je:
. Enačba je:
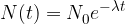
pri čemer sta 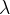 in
in 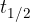 povezana s faktorjem naravnega logaritma od 2:
povezana s faktorjem naravnega logaritma od 2:
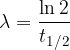
Tri najpogostejše in najprej odkrite vrste radioaktivnega razpada so:
razpad alfa (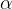 ),
),
razpad beta (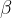 ),
),
razpad gama (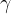 ).
).
Poglejmo si jih natančneje.
Pri razpadu alfa začetno jedro razpade na:
delec alfa, ki je sestavljen iz dveh protonov in dveh nevtronov in
končno jedro, ki je zmanjšano za dva protona in dva nevtrona.
Atomsko jedro ob razpadu preide na nižje energetsko stanje. Pri razpadu jedra nastane tudi "odvečna energija", ki se sprosti kot:
kinetična energija delca alfa in
kinetična energija jedra.
Ker pa je jedro ponavadi mnogo težje od delca alfa, večino kinetične energije prejme delec alfa.
Kot rečeno, z oddajo delca alfa jedro izgubi dva protona in dva nevtrona. Zato se jedru zmanjša:
vrstno število Z za dve
masno število A za štiri.
Začetno jedro se zato pretvori v nov element.
Pri razpadu beta začetno jedro razpade na:
elektron,
nevtrino,
končno jedro, v katerem se en nevtron spremeni v proton.
Ker v jedru iz nevtrona nastane proton, jedro - da ohrani skupni naboj - odda še negativen beta delec, ki je elektron. Poleg tega pri razpadu nastane še delec brez mase in brez naboja, ki ga imenujemo nevtrino in označimo kot 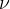 .
.
Pri tem se jedru:
ohrani masno število A,
za 1 pa se poveča vrstno število Z.
Reakcijo lahko zapišemo kot:
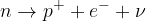
Energija, ki se sprosti pri razpadu, se večinoma pretvori v kinetično energijo elektrona in nevtrina.
Gama aktivno jedro odda svoj energijski presežek z izsevanjem fotona gama. Pri tem se sestava jedra ne spremeni.
Aktivnost snovi je določena s številom razpadov na sekundo. Aktivnost je tem večja:
tem večja je količina snovi ali / in
tem večja je hitrost razpada jeder.
Aktivnost označimo z 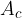 in izračunamo po formuli:
in izračunamo po formuli:
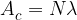
kjer je lambda (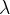 ) razpadna konstanta in N število jeder, ki razpadajo. Enota za aktivnost je:
) razpadna konstanta in N število jeder, ki razpadajo. Enota za aktivnost je:
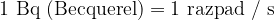
Kot zanimivost dodajmo, da je bila stara enota za aktivnost definirana kot aktivnost enega grama radija 226. Imenovala se je Curie. Staro in novo enoto povezuje enačba: