Osebne zbirke


Velika večina lastnostih, ki jih kažejo organske spojine, je posledica sil, ki se ustvarjajo med posameznimi molekulami. Med temi silami je najbolj vplivna vodikova vez. To je vez, ki na primer povzroči, da ima snov iz nekega tipa molekul višje vrelišče, kot bi ga lahko napovedali iz molekulske mase.
Spomnimo se: večje kot so molekule (večja molekulska masa), več medmolekulskih sil lahko tvorijo. Iz tipa in števila medmolekulskih sil pa lahko napovemo temperaturo vrelišča snovi.
Vodikova vez je močna medmolekularna vez, ki nastane samo med določenimi atomi sosednjih molekul. V tej vezi se vodik poveže s:
kisikom,
dušikom,
fluorom.
Vodikova vez nastane med:
vodikom, ki je vezan na enega izmed treh najbolj elektronegativnih atomov (F,O,N) in
kisikom, dušikom ali fluorom v sosednji molekuli.
Poglejmo si primer vodikove vezi med molekulama vode.
V organski kemiji poznamo veliko spojin, ki vsebujejo tako kisik kot tudi dušik:
kisikove organske spojine (alkoholi, etri, ketoni, aldehidi, kisline)
dušikove organske spojine (amini, amidi)
Vedno manj pogosto pa se srečujemo z organskimi spojinami, ki vsebujejo fluor.
Fluorovih spojin se izogibamo predvsem zato, ker so veliki onesnaževalci okolja in negativno vplivajo na ozon. Spomnimo se samo CFC (klorofluoroogljikovodiki) spojin, t.i. freonov.
V nadaljevanju si poglejmo, katere izmed kisikovih in dušikovih spojin se lahko med seboj povezujejo z vodikovo vezjo.
Značilnost kisikovih organskih spojin (kot so alkoholi, aldehidi, ketoni, kisline...) je, da v svoji strukturi vsebujejo kisikove atome.
Kisikove organske spojine, ki se lahko povežejo z vodikovo vezjo, so:
alkoholi,
kisline.
Spomnimo se: Vodikova vez nastane samo takrat, ko je vodik vezan na enega izmed najbolj elektronegativnih atomov in se lahko poveže s sosednjo molekulo. V alkoholih in kislinah je vodik vezan na kisik. Poglejmo si vodikove vezi v teh spojinah.
Alkoholi imajo v svoji strukturi hidroksilno skupino (OH).
Hidroksilna skupina ima izredno podobno strukturo kot voda.
In podobno kot v vodi je tudi tukaj eden izmed vodikov vezan neposredno na kisik.
Ker je kisik bolj elektronegativen (bolj privlači elektrone k sebi), se elektroni nahajajo bližje kisikovemu jedru. Rečemo, da kisik pobere elektron tistemu vodiku, s katerim tvori vez. Zato tak vodik poišče elektrone drugje. Najde ga lahko v neveznih parih kisikovih atomov sosednjih molekul.
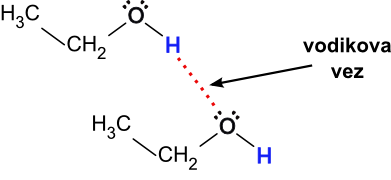
Slika 6: Vodikova vez v alkoholu nastane med vodikom iz hidroksilne skupine in kisikom sosednje molekule.
Podobno kot alkoholi, imajo tudi:
etri,
v svoji strukturi prisoten kisikov atom (glej sliko 7).
Vendar pa na teh kisikovih atomih ni vezanega vodika (tvorijo vezi izključno z ogljiki) zato se te molekule ne morejo povezovati med seboj z vodikovo vezjo.
Primer: Vodikova vez med molekulami etra ni mogoča, ker manjka vodik vezan na enega izmed treh najbolj elektronegativnih atomov.
Organske kisline imajo v svoji strukturi karboksilno skupino (COOH), ki je primerna za tvorbo vodikovih vezi.
Tudi ta skupina ima enega od vodikov vezanega na kisikov atom.
Zato so se tudi karboksilne skupine organskih kislin sposobne povezovati med seboj z vodikovo vezjo.
Estri (slika 12) imajo v svoji strukturi dva kisika (podobno kot organske kisline), vendar na teh kisikih nimamo vezanih vodikov.
Zato se estri niso zmožni povezovat med seboj z vodikovimi vezmi.
Amini in amidi spadajo med in dušikove organske spojine. To so spojine, ki imajo v svoji strukturi vključene dušikove atome.
Amini so spojine, ki imajo v strukturi amino skupino.
Amino skupina pa je zelo podobna strukturi amonijaka.
Kot amoniak, imajo tudi amini vodike (modro označeni) vezane na dušik.
In taki vodiki se lahko povežejo na dušik v sosednji molekuli z vodikovo vezjo.
Podobno kot amini imajo tudi amidi skupino (amidna skupina -CONH-), ki vsebuje vodik vezan na dušikov atom.
Tak vodik se je zato sposoben povezati s sosednjo molekulo z vodikovo vezjo.
Piridin in njemu podobne dušikove spojine (slika 21) pa nimajo vodika vezanega na dušikov atom (kot amini in amidi). Zato se med seboj niso sposobne povezovati z vodikovo vezjo.